II. Aufbau einer PEM-Einzelzelle
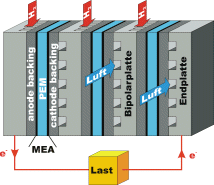
III. Der PEMFC-Stack
IV. Eigenschaften der PEMFC
I. Funktion einer Brennstoffzelle (allgemein)
I. 1. Chemie der Brennstoffzelle
In einer Brennstoffzelle (BZ) erfolgt eine kontrollierte Oxidation des in der Regel gasförmigen Brennstoffs, meist Wasserstoff, mit Sauerstoff oder Luft. Der wichtigste Unterschied zur bekannten Knallgasreaktion (H2 + 1/2 O2 → H2O), bei der Wasserstoff mit Sauerstoff unter heftiger Explosion zu Wasser reagieren, ist der, dass die Oxidation des Wasserstoffs und die Reduktion des Sauerstoffs durch einen Elektrolyten räumlich voneinander getrennt sind.
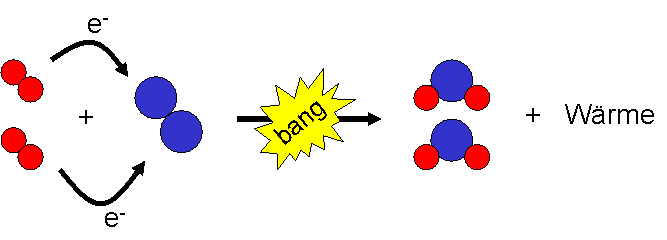
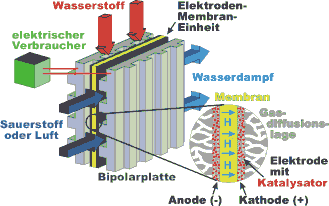
Durch diese Trennung findet kein direkter Elektronentransfer vom Wasserstoff zum Sauerstoff (wie in der Knallgasreaktion), sondern ein indirekter Elektronentransfer statt. Die Elektronen werden über zwei Elektroden am Elektrolyten (hier gelb dargestellt) "vorbeigeleitet". Auf diese Weise kann ein Teil der im Wasserstoff gespeicherten chemischen Energie als elektrische Energie genutzt werden. Der Ladungsausgleich erfolgt durch einen Ionentransport (hier Protonentransport) durch den Elektrolyten.
Das Kernstück einer jeden BZ ist der Elektrolyt. Deshalb werden die einzelnen BZ-Typen auch nach der Art der verwendeten Elektrolyten unterschieden. In der PEMFC besteht der Elektrolyt aus einer protonenleitenden Membran. Auf der Membran sind die beiden Elektroden (Anode und Kathode) aufgebracht. An der Anode wird Wasserstoff durch einen geeigneten Edelmetall-Katalysator (z. B. Pt) zu Protonen oxidiert (engl.: hydrogen oxidation reaction, HOR) und gibt jeweils sein Elektron ab:
H2 → 2 H+ + 2 e-
Die Anode bildet den Minus-Pol einer Zelle, da hier die Elektronen aus dem System ausgeführt werden. Die Protonen wandern von der Anode durch die Membran (zum Beispiel einem Polymer aus Poly-perfluorsulfonsäure) zur Kathode. An der Katode, dem Plus-Pol, werden die Elektronen wieder dem System zugeführt. Dadurch diese Elektronen wird der an der Kathode bereitgestellte Sauerstoff reduziert (engl.: oxygen reduction reaction, ORR) und nimmt die durch den Elektrolyten gewanderten Protonen auf. Bei dieser Reaktion entsteht das Produktwasser.
1/2 O2 + 2 e- + 2 H+ → H2O
Die Gesamtreaktion einer H2/O2-BZ lautet demnach:
H2 + 1/2 O2 → H2O
Ganz allgemein erfolgt der für den Ablauf der chemischen Reaktion in der Brennstoffzelle notwendige Ladungsausgleich durch die Wanderung von Ionen durch den Elektrolyten. Je nach BZ-Typ kann der Elektrolyt sauren oder basischen Charakter haben. In sauren Elektrolyten erfolgt der Ladungsausgleich durch die Wanderung von Protonen und in basischen Elektrolyten durch Wanderung von Oxidionen (oder gebunden in Carbonationen).
I. 2. Volumenstrom, Gasumsatz und Stöchiometrie
Nach dem Faraday´chen Gesetz (n = Q/zF) lässt sich der Gasbedarf einer Einzelzelle als Molenstrom φmol berechnen:
φmol = 1 / zF ![]() [φmol] = mol/ As
[φmol] = mol/ As
Dabei ist F die Faraday-Konstante (F = 96485,3 As/mol) und z die Anzahl der ausgetauschten Elektronen (z = 2 bei obiger Reaktion). Sinnvoller als die molare Größe ist die Angabe als Volumenstrom φ in Normliter pro Ampere und Minute (Nl/A min). Die Umrechnung erfolgt über das Molvolumen eines idealen Gases (Vmol = V/n = RT/p = 22,414 Nl/mol) unter Normbedingungen (101325 Pa, 0°C oder 273,15K).
φ = φ mol ·
Vmol · 60s/min ![]() [φ] = Nl/ A min
[φ] = Nl/ A min
Durch die Umrechnung in Volumenströme werden diese Berechnungen abhängig von Druck und Temperatur. Die auf Normbedingungen (s. o.) bezogenen Volumenströme müssen deswegen in Normlitern angegeben werden (engl.: standard liter per minute, slpm).
Durch Einsetzen erhält man folgende Werte für Wasserstoff und Sauerstoff pro Einzelzelle:
φH2 = 7,0·10-3 Nl/A min und φ O2 = 3,5·10-3 Nl/A min
Wenn die BZ mit Luft an Stelle von reinem Sauerstoff betrieben wird, muss durch den Molenbruch (x = 0,21) geteilt werden, da 21 Vol.% Sauerstoff in Luft enthalten sind:
φLuft = 16,6·10-3 Nl/A min.
Dieser theoretische Gasbedarf für Anode und Kathode entspricht einer Stöchiometrie von λ = 1 bzw. einem 100%igen Gasumsatz u. Dabei gilt folgender Zusammenhang zwischen dem Umsatz u und der Stöchiometrie λ:
λ = 1/u
In der Praxis ist der Umsatz immer kleiner als 100% (u < 100%) bzw. die Stöchiometrie größer als eins (λ > 1), da die BZ die bereitgestellten Reaktionsgase nie vollständig umsetzen kann. Das bedeutet, dass mehr Wasserstoff bzw. Sauerstoff oder Luft für den Betrieb einer Zelle bereitgestellt werden müssen als der Theorie nach berechnet. Wenn doppelt so viel Gas bereitgestellt wird, entspricht das einem Umsatz von u = 50% oder einer Stöchiometrie von λ = 2. Der für den Betrieb einer Einzelzelle notwendige Gasbedarf im H 2/Luft-Betrieb berechnet sich deshalb nach folgender Formel:
Anode: φH2 =
λanode · 7,0·10-3 Nl/A min
Kathode:
φLuft = λcathode · 16,6·10-3
Nl/A min
Die Stöchiometrie, mit der ein BZ-Stack betrieben werden kann, ist von vielen Faktoren abhängig (Gaszusammensetzung, Flowfield, Wassermanagement, ...). Um in einem BZ-System einen guten Wirkungsgrad (siehe unten) zu erreichen, muss auf der Anodenseite eine möglichst niedrige Stöchiometrie (hoher Umsatz) an Wasserstoff gefahren werden. Dabei wird zwischen Bruttoumsatz und Single-Pass-Umsatz unterschieden. Der Bruttoumsatz ist der Umsatz, der sich auf das BZ-System bezieht. Der Single-Pass-Umsatz dagegen bezieht sich auf den BZ-Stack. Wenn das BZ-System mit einer Anodenumwälzung (Anodenrezirkulation) betrieben wird, können Brutto- und Single-Pass-Umsatz verschieden sein. Mehr dazu unter BZ-System. Realistisch sind Werte λanode ≤ 1,5 (Single-Pass-Umsatz). Die Stöchiometrie auf der Kathodenseite liegt beim Luftbetrieb oft zwischen 1,5 ≤ λcathode ≤ 4.
I. 3. Thermodynamik der Brennstoffzelle
Die maximale Arbeit, die von einem System geleistet werden kann, ist durch die freie Gibbs´ Enthalpie ΔG gegeben. Wenn Temperatur und Druck konstant sind (∂T = 0 und ∂p = 0), dann kann bei einer elektrochemischen Reaktion die maximale Arbeit als elektrische Spannung genutzt werden. Diese Spannung nennt man Elektromotorische Kraft (EMK) , Gleichgewichtspannung oder Ruhespannung. Entsprechend dem Potential der obigen Reaktion berechnet sich die Einzelzellspannung UEZ,0 der H2/O2-BZ wie folgt:
UEZ, 0 = -ΔG / zF
Dabei ist F die Faraday-Konstante (F = 96485,3 As/mol) und z die Zahl der ausgetauschten Elektronen (hier z = 2).
Für die weiteren Betrachtungen muss nun zwischen dem Brennwert (früher oberer Heizwert, englisch upper heating value UHV) und dem Heizwert (früher unterer Heizwert, englisch lower heating value LHV) von Wasserstoff unterschieden werden. Der Brennwert liegt dabei immer über dem Heizwert. Der Brennwert bzw. Heizwert eines Brennstoffes entspricht der Reaktionsenthalpie ΔHR der chemischen Reaktion, bei der der Brennstoff mit Sauerstoff oxidiert wird und Wasser entsteht. Fällt dieses Produktwasser flüssig an, spricht man vom Brennwert ΔHo des Brennstoffs. Wenn das Produktwasser gasförmig anfällt, spricht man vom Heizwert ΔHu. Der Betrag von ΔHo ist um den Betrag der Verdampfungsenthalpie des Wassers ΔHverd größer als |ΔHu|.
Für Wasserstoff und damit für die H2/O2-BZ bedeutet das bei Standardbedingungen (25°C, 1 bar):
Heizwert: H2 + 1/2 O2 → H2O(g)
![]() ΔHu = -241,82 kJ/mol
ΔHu = -241,82 kJ/mol
![]() (mit ΔGu = -228,57 kJ/mol)
(mit ΔGu = -228,57 kJ/mol)
bzw.
Brennwert: H2 + 1/2 O2 → H2O(l)
![]() ΔHo = -285,83 kJ/mol
ΔHo = -285,83 kJ/mol
![]() (mit ΔGo = -237,41 kJ/mol)
(mit ΔGo = -237,41 kJ/mol)
Aus diesem Grund ist es wichtig, bei allen weiteren Betrachtungen immer den Bezug auf den Brenn- oder Heizwert anzugeben.
Die maximale, theoretische Zellspannung oder EMK der H2/O2-BZ beträgt damit nach obiger Gleichung UEZ,0 = 1,229V (bezogen auf ΔHo) und UEZ,0 = 1,184V (bezogen auf ΔHu).
Den Zusammenhang zwischen ΔH und ΔG beschreibt die Gibbs-Helmholtz-Gleichung
ΔG = ΔH - TΔS.
Da bei der chemischen Reaktion in der H2/O2-BZ ΔS negativ ist, obige Reaktion aber spontan abläuft, muss der Entropieterm TΔS in Form von Wärme (thermischer Energie) an die Umgebung abgeführt werden. Der Entropietherm wird auch als reversible Wärmetönung bezeichnet. Dieser Teil der chemischen Energie, der (laut Thermodynamik) nicht in Arbeit und damit auch nicht in elektrische Energie umgewandelt werden kann, fällt also in Form von Wärme bei der BZ-Reaktion an.
Aus der Gibbs-Helmholtz-Gleichung ergibt sich eine lineare Abnahme der Einzelzellspannung mit zunehmender Temperatur (In einem kleinen Temperaturbereich können ΔG, ΔH und ΔS als temperaturunabhängig betrachtet werden!). Bei 800°C beträgt die Zellspannung nur noch UEZ,0 = 1,046V (bezogen auf ΔH u).
I. 4. Kinetik der Brennstoffzelle
Die bisherige thermodynamische Betrachtung gilt nur, solange sich das System im Gleichgewicht befindet. Sobald der Stromkreis mit einer BZ und einem elektrischen Verbraucher geschlossen wird, fließt ein Strom und es treten elektrische Verluste in Form von Überspannungen (elektrochemische "Reibung") auf. Diese Überspannungen verringern die Spannung der BZ, und zwar zum so stärker, je höher die Stromstärke I (bzw. Stromdichte j) ist. Die Stromdichte berechnet sich aus der Stromstärke I und der aktiven Elektrodenfläche A:
j = I / A ![]() [j] = A/cm2
[j] = A/cm2
Überspannungen sind das Ergebnis von kinetisch gehinderten Elektrodenreaktionen und führen zu mehr oder weniger hohen Verlusten. Zusätzlich zu den Entropieverlusten (s. o.) wird durch Überspannungen ein Teil der chemischen Energie als Wärme abgegeben und kann dadurch nicht mehr als elektrischer Energie genutzt werden.
Einige Überspannungen zeigen ein nichtlineares Verhalten.
Dadurch ergibt sich ein typischer Kurvenverlauf für die
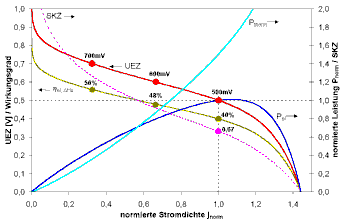
Strom-Spannungs-Kennlinie (englisch polarization curve oder PolCurve) einer BZ. Bei dieser Kennlinie wird die
Einzelzellspannung UEZ(j) (Klemmspannung) in
Abhängigkeit der Stromdichte j aufgezeichnet. In der
nächsten Abbildung ist der typische Verlauf einer solchen
U-I-Kennlinie dargestellt (rote Kurve). Die offene Zellspannung (open
cell voltage, OCV) ist die Leerlaufspannung einer BZ, also diejenige
Einzelzellspannung, die ohne Stromfluss gemessen wird. In der Praxis
werden Werte zwischen 950 und 1000mV gemessen. Warum ist die OCV
niedriger als die EMK? Die Ursache liegt in der sogenannten
Ruhepolarisation, die unter anderem verursacht wird durch
a)
Mischpotential im H2O2-Pfad (E0 =
0,67V),
b) Bildung von Platinoxid bei Potentialen > 0,8V,
c)
Diffusion von H2 durch Membran.